
Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.
บริษัท Suyzeko ได้ทำการวิจัยผลิตภัณฑ์ใหม่ เครื่อง photobiomodulation สมอง บริษัท ของเราใช้เวลามากกว่า 1 ปีในการค้นคว้าผลิตภัณฑ์และเราเชิญศาสตราจารย์ให้ทำวิจัยให้เรา ดูบทความต่อไปนี้สำหรับรายละเอียด
หน่วยวิจัยสำหรับการแพทย์เลเซอร์เสริมและบูรณาการหน่วยวิจัยของวิศวกรรมชีวการแพทย์ในการดมยาสลบและการแพทย์ผู้ป่วยหนักและศูนย์วิจัย TCM GRAZ, Medical University of Graz, Auenbruggerplatz 39, EG19, 8036 GRAZ, ออสเตรีย, ออสเตรีย, ออสเตรีย
ได้รับ: 4 มกราคม 2019 / ยอมรับ: 15 มกราคม 2019 / เผยแพร่: 16 มกราคม 2019
Photobiomodulation; สมอง; การกระตุ้น LED (ไดโอดเปล่งแสง); การบำบัดด้วยแสง; ความยาวคลื่น; จังหวะ; ภาวะสมองเสื่อม; โรคทางจิต; ความอิ่มตัวของออกซิเจนในสมองในภูมิภาค การถ่ายภาพความร้อน หมวกกันน็อก LED
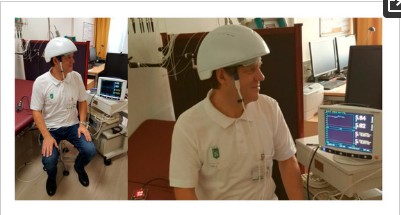
รูปที่ 1 การวัดครั้งแรกด้วยหมวกกันน็อก LED (Light Emitting Diode) หมวกกันน็อกโฟโตไบโอโมดอเรนต์ (ต้นแบบจาก Suyzeko (Shenzhen Guangyang Zhongkang Technology Limited, China) ที่ศูนย์วิจัย TCM ที่มหาวิทยาลัย Medical of Graz, ออสเตรีย, ยุโรปดำเนินการเมื่อวันที่ 25 ธันวาคม 2018 .
ปัจจุบันอุปกรณ์ขึ้นอยู่กับ LED อินฟราเรดโดยใช้ความยาวคลื่น 810 นาโนเมตร ความยาวคลื่นนี้ได้รับการพิสูจน์เมื่อเร็ว ๆ นี้ (2018) เป็นหนึ่งในสิ่งที่ดีที่สุดสำหรับการกระตุ้นด้วยเลเซอร์/แสง transcranial [9] ผลลัพธ์ได้รับการยืนยันโดยการวัดที่ดำเนินการโดยทีมวิจัยของเรา [5,6,7,8,10]

การวัดการเปลี่ยนแปลงของความอิ่มตัวของออกซิเจนในสมองในภูมิภาค (RSO2) ได้ดำเนินการโดยใช้ InvOS 5100C oximeter (Somanetics Corp. , Troy, MI, USA) ใกล้กับอินฟราเรดสเปกโทรสโกปีเป็นวิธีที่ไม่รุกล้ำสำหรับการวัด RSO2through กะโหลกศีรษะที่ไม่บุบสลายซึ่งได้รับการใช้งานอย่างประสบความสำเร็จในการวิจัยทางการแพทย์ขั้นพื้นฐานและข้อบ่งชี้ทางคลินิกเป็นเวลาหลายปี [6] แสงใกล้อินฟราเรด (730 และ 805 นาโนเมตร) ถูกปล่อยออกมาผ่านผิวหนังและหลังจากผ่านเนื้อเยื่อชนิดต่าง ๆ (ผิวหนังและกระดูก) แสงที่ส่งคืนจะถูกตรวจพบในระยะทางสองระยะทางจากแหล่งกำเนิดแสง (3 และ 4 ซม.) ขึ้นอยู่กับหลักการนี้การดูดซึมสเปกตรัมของเลือดในโครงสร้างที่ลึกกว่า (2–4 ซม.) สามารถกำหนดและกำหนดเป็น RSO2 [5,12] เซ็นเซอร์ถูกนำไปใช้ในพื้นที่ด้านหน้าทางด้านขวาและด้านซ้ายของสมองของอาสาสมัครที่มีสุขภาพดี (ดูรูปที่ 1) เพื่อลดอิทธิพลของแสงภายนอกหัวในพื้นที่นี้ถูกปกคลุมด้วยแถบยืดหยุ่นในระหว่างขั้นตอนการบันทึกและการกระตุ้น หลังจากเวลาพัก 20 นาทีการกระตุ้น LED ก็เปิดอยู่ ผลลัพธ์ของสามส่วน (ก่อน (20 นาที) ระหว่าง (15 นาที) และหลังจากการกระตุ้น (20 นาที)) จะถูกระบุในรูปที่ 3 หมายเหตุการเพิ่มขึ้นอย่างมีนัยสำคัญใน RSO2 (ด้านซ้ายและขวา) ในระหว่างและแม้กระทั่งหลัง transcranial การกระตุ้น LED การเปลี่ยนแปลงของอุณหภูมิแสดงในรูปที่ 4
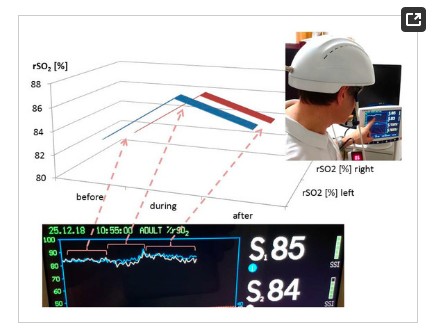
รูปที่ 3 ผลลัพธ์ของการวัดนักบินครั้งแรกด้วยหมวกกันน็อกการกระตุ้น LED จาก Suyzeko (เซินเจิ้น, จีน) สังเกตการเพิ่มขึ้นของความอิ่มตัวของออกซิเจนในสมองในภูมิภาคระหว่างและหลังการกระตุ้นทางด้านซ้ายและขวา

การรักษาด้วย PBM ได้รับการพัฒนามานานกว่า 50 ปีแล้ว อย่างไรก็ตามยังไม่มีข้อตกลงร่วมกันเกี่ยวกับพารามิเตอร์และโปรโตคอลสำหรับการใช้งานทางคลินิก ทีมวิจัยบางคนแนะนำให้ใช้ความหนาแน่นของพลังงานน้อยกว่า 100 mW/cm2 และความหนาแน่นของพลังงาน 4 ถึง 10 J/cm2 [11] กลุ่มอื่น ๆ แนะนำให้มากถึง 50 J/cm2 ที่พื้นผิวเนื้อเยื่อ [11] พารามิเตอร์เช่นความยาวคลื่นพลังงานความคล่องแคล่วพลังงานการฉายรังสีโหมดชีพจรระยะเวลาการรักษาและอัตราการทำซ้ำสามารถใช้ในช่วงกว้าง ผลลัพธ์เบื้องต้นของเราในปัจจุบันแสดงให้เห็นถึงการตอบสนองที่ชัดเจนของสมอง RSO2 ที่เกี่ยวข้องกับการกระตุ้น LED อย่างไรก็ตามจะต้องมีการกล่าวถึงว่าอุณหภูมิเพิ่มขึ้นอย่างมีนัยสำคัญและผลกระทบเหล่านี้จะต้องนำมาพิจารณาในการศึกษาเพิ่มเติมในรายละเอียด นอกจากนี้ยังมีข้อเท็จจริงที่ว่าการศึกษาที่ไม่มีประสิทธิภาพในเซลล์ที่มีกิจกรรมไมโตคอนเดรียสูงดูเหมือนจะเกิดขึ้นบ่อยกว่าการใช้ยาเกินกว่าที่จะลดลง [11] ดังนั้นการศึกษาทางคลินิกที่เกี่ยวข้องกับปริมาณการกระตุ้นที่ดีที่สุดจึงเป็นสิ่งจำเป็น
Transcranial PBM ปรากฏว่ามีแนวโน้มที่จะรักษาโรคทางจิตที่แตกต่างกัน Pitzschke และคณะ [13] นอกจากนี้ยังวัดการแพร่กระจายของแสงในพื้นที่ต่าง ๆ ของโรคพาร์กินสัน (PD)-เนื้อเยื่อสมองส่วนลึกที่เกี่ยวข้องในระหว่างการส่องสว่าง transcranial และ transsphenoidal (ที่ 671 และ 808 nm) ของหัวซากศพและพารามิเตอร์แสงแบบจำลองของเนื้อเยื่อสมองมนุษย์มนุษย์ การจำลองคาร์โล การศึกษาครั้งนี้แสดงให้เห็นว่าเป็นไปได้ที่จะส่องสว่างเนื้อเยื่อสมองลึก transcranially และ transsphenoidally สิ่งนี้เปิดตัวเลือกการรักษาสำหรับผู้ประสบภัย PD หรือโรคสมองอื่น ๆ ที่จำเป็นต้องใช้การรักษาด้วยแสง [13]
มีการตรวจสอบหลายประการเกี่ยวกับผลข้างเคียงที่เป็นไปได้สำหรับ LED PBM ตัวอย่างเช่น Moro และคณะ สำรวจผลกระทบของการใช้งานในระยะยาวนานถึง 12 สัปดาห์ของ PBM (670 nm) ในลิง macaque ที่ไร้เดียงสา พวกเขาไม่พบพื้นฐานทางเนื้อเยื่อวิทยาสำหรับข้อกังวลด้านความปลอดภัยทางชีวภาพที่สำคัญใด ๆ ที่เกี่ยวข้องกับ PBM ที่ส่งโดยวิธีการในกะโหลกศีรษะ [14] Hennessy และ Hamblin ยังชี้ให้เห็นถึงความปลอดภัยที่จัดตั้งขึ้นแล้วและการขาดผลกระทบที่ไม่พึงประสงค์จาก Transcranial PBM [2]
ผลลัพธ์เบื้องต้นมีแนวโน้มมาก อย่างไรก็ตามจำเป็นต้องมีงานวิจัยเพิ่มเติมเพื่อให้สามารถใช้งานได้เช่น PBM รูปแบบใหม่นี้เป็นวิธีการรักษา นักวิจัยหลายคนเชื่อว่า PBM ที่มี LED และ/หรือเลเซอร์สำหรับความผิดปกติของสมองจะกลายเป็นหนึ่งในแอพพลิเคชั่นทางการแพทย์ที่สำคัญที่สุดของการรักษาด้วยแสงในอีกไม่กี่ปีข้างหน้าและหลายทศวรรษที่ผ่านมา [3]
ผู้เขียนประกาศว่าไม่มีความขัดแย้งทางผลประโยชน์
Author:
Mr. Arvin Jiang
อีเมล:
August 17, 2024
December 01, 2023
November 14, 2023
อีเมล์ให้ผู้ขายนี้
Author:
Mr. Arvin Jiang
อีเมล:
August 17, 2024
December 01, 2023
November 14, 2023

Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.

Fill in more information so that we can get in touch with you faster
Privacy statement: Your privacy is very important to Us. Our company promises not to disclose your personal information to any external company with out your explicit permission.